欢迎光临药得网站!
erdafitinib tablets/盼樂/BALVERSA tablets
片剂
3 mg*56片:4 mg*56片;5 mg*28片
36个月
Janssen Pharmaceutical Companies
瑞士
详询客服
【临床数据】
1 具有易感 FGFR3 基因改变的尿路上皮癌
BALVERSA 的疗效在研究 BLC3001 (NCT03390504) 队列 1 中进行了评估,该研究是一项随机、开放标签、多中心研究,其中 266 名患有选定的 FGFR3 基因改变的晚期尿路上皮癌患者按 1:1 随机分组至 接受 BALVERSA(8 mg,增加至 9 mg)与化疗(多西紫杉醇 75 mg/m2,每 3 周一次,或vinflunine 320 mg/m2,每 3 周一次)相比,直至出现不可接受的毒性或进展。
表 9 以及图 1 和图 2 总结了 BLC3001 队列 1 的疗效结果。
表 9:BLC3001 研究第 1 组的疗效结果

a 基于 Kaplan-Meier 估计
b 基于非分层 Cox 比例风险模型
c 基于非分层对数秩检验
d p 值使用 Cochran-Haenszel (CMH) 检验进行估计,并以 ECOG 表现状态(0 或 1 vs 2)作为分层因子。
图 1:总体生存率的 Kaplan-Meier 图(研究 BLC3001 队列 1)

图 2:无进展生存期的 Kaplan-Meier 图(研究 BLC3001 队列 1)

研究 BLC3001 队列 2
研究 BLC3001 (NCT03390504) 队列 2 是一项多中心、开放标签、随机研究,受试者为 351 名局部晚期或转移性尿路上皮癌患者,这些患者具有选定的 FGFR3 改变,且既往接受过 1 线全身治疗,且未接受过 PD-1 或PD-L1抑制剂治疗。
患者按照 1:1 的比例随机接受 BALVERSA(8 mg,增加至至 9 mg)或帕博利珠单抗 200 mg,每 3 周一次。 在预先指定的最终分析中,该研究未达到 OS 优越性的主要疗效结果指标。 BALVERSA 的 OS 风险比 (HR) 为 1.18 (95% CI: 0.92, 1.51; p=0.18),中位数为 10.9 (95% CI: 9.2, 12.6) 个月,而帕博利珠单抗组的中位数为 11.1 (95% CI: 9.7, 13.6) 个月。
研究BLC2001
研究 BLC2001 (NCT02365597) 是一项多中心、开放标签、单臂研究,旨在评估 BALVERSA 对局部晚期或转移性尿路上皮癌 (mUC) 患者的疗效和安全性。 通过临床试验测定 (CTA) 确定用于筛选和登记患者的 FGFR 突变状态。
疗效结果总结于表10和表11中。ORR为32.2%。 有反应者包括先前对抗 PD-L1/PD-1 治疗没有反应的患者。
表 10:疗效结果
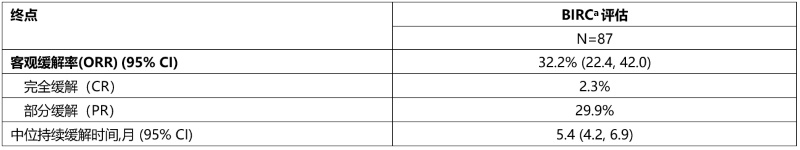
a BIRC:盲态独立审查委员会
表 11:FGFR 基因改变的疗效结果

a BIRC:盲态独立审查委员会
b 两名应答者均具有 FGFR3-TACC3_V1 融合
c 上述 FGFR2 融合和 FGFR3 融合均报告了一名具有 FGFR2-CASP7/FGFR3-TACC3_V3 融合的患者
免责声明:由本文所表达的任何关于疾病的建议都不应该被视为医生的建议或替代品,请咨询您的治疗医生了解更多细节。本站信息仅供参考,药得不承担任何责任。